Phản ứng giữa Na2S và KOH là một chủ đề thú vị trong hóa học vô cơ, liên quan đến sự tương tác giữa muối natri sunfua (Na2S) và bazơ kali hydroxit (KOH). Bài viết này sẽ đi sâu vào phân tích phản ứng này, từ cơ chế đến ứng dụng thực tiễn.
Na2S + KOH: Cơ chế phản ứng
Vậy khi kết hợp Na2S và KOH, điều gì xảy ra? Thực tế, trong dung dịch nước, cả Na2S và KOH đều phân ly hoàn toàn thành các ion. Na2S tạo ra ion Na+ và S2-, trong khi KOH tạo ra ion K+ và OH-. Phản ứng giữa Na2S và KOH không tạo ra sản phẩm mới, mà bản chất là sự hòa tan của hai chất điện li mạnh trong nước. 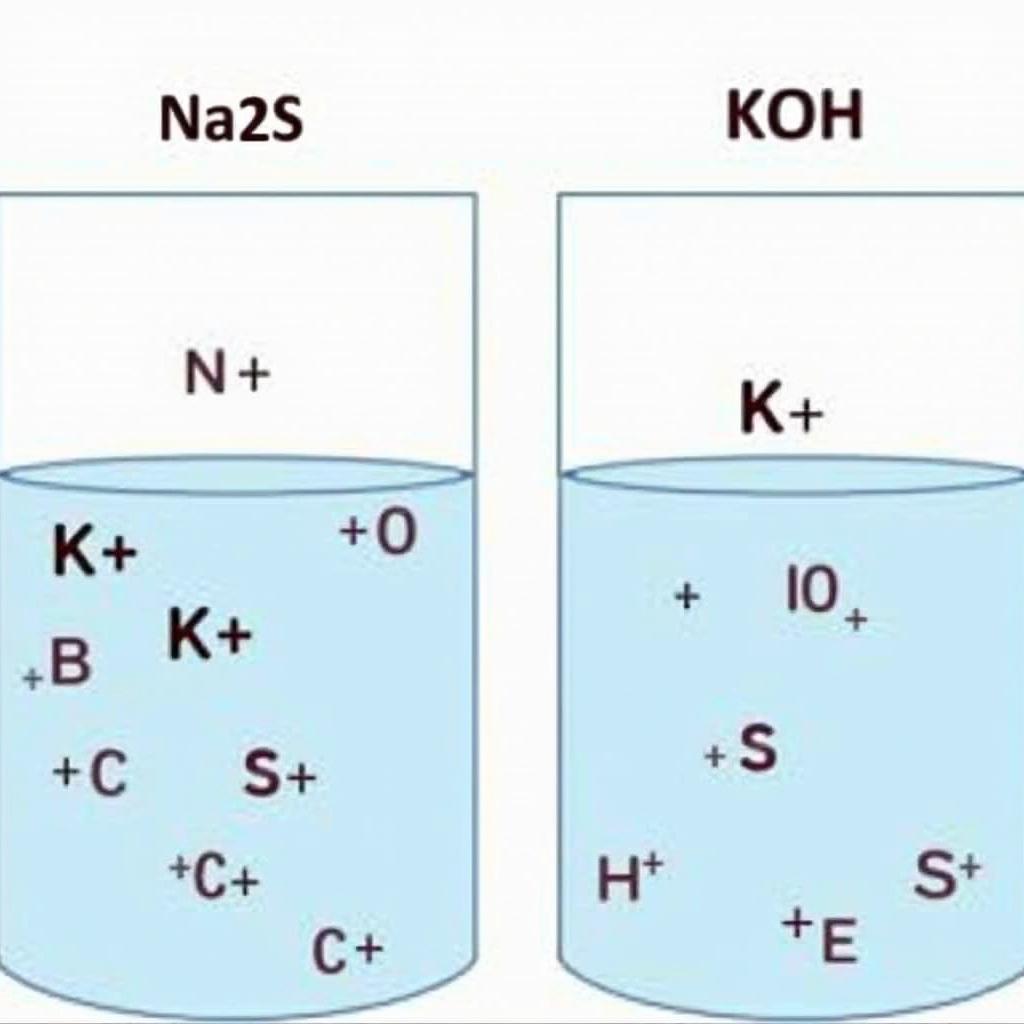 Phản ứng Na2S và KOH
Phản ứng Na2S và KOH
S2- + H2O <=> HS- + OH-
HS- + H2O <=> H2S + OH-
Do S2- là bazơ liên hợp của axit yếu H2S nên nó có tính bazơ. Trong dung dịch, S2- sẽ bị thủy phân tạo thành HS- và OH-. Chính sự xuất hiện của OH- khiến cho dung dịch có tính bazơ. bài 7 tính chất hóa học của bazơ Việc thêm KOH, một bazơ mạnh, vào dung dịch Na2S sẽ làm tăng nồng độ OH-, làm cân bằng phản ứng thủy phân của S2- chuyển dịch sang trái, giảm sự thủy phân của S2-.
Ứng dụng của Na2S và KOH trong thực tế
Cả Na2S và KOH đều là những hóa chất quan trọng với nhiều ứng dụng trong công nghiệp. Na2S được sử dụng trong sản xuất thuốc nhuộm, thuộc da và tách kim loại. KOH, một bazo manh, được sử dụng rộng rãi trong sản xuất xà phòng, phân bón và pin. Mặc dù không phản ứng trực tiếp với nhau, việc hiểu rõ tính chất của từng chất là rất quan trọng để ứng dụng chúng một cách hiệu quả.
Những câu hỏi thường gặp về Na2S và KOH
Na2S có phản ứng với KOH không?
Như đã phân tích, Na2S và KOH không phản ứng hóa học với nhau trong dung dịch nước.
Dung dịch Na2S có tính gì?
Dung dịch Na2S có tính bazơ do sự thủy phân của ion S2-.
KOH có phải là bazơ mạnh không?
Đúng vậy, KOH là một bazơ mạnh, phân ly hoàn toàn trong nước.
Na2S được sử dụng để làm gì?
Na2S được sử dụng trong nhiều ngành công nghiệp, bao gồm sản xuất thuốc nhuộm, thuộc da và tách kim loại.
KOH có ứng dụng gì trong đời sống?
KOH được sử dụng trong sản xuất xà phòng, phân bón và pin. axit bazơ
Na2S và KOH: Kết luận
Tóm lại, Na2S và KOH không phản ứng hóa học với nhau. Việc hiểu rõ tính chất và ứng dụng của từng chất là rất quan trọng trong việc sử dụng chúng một cách an toàn và hiệu quả. phương pháp xử lý khí no2 trong phòng thí nghiệm Hi vọng bài viết này đã cung cấp cho bạn cái nhìn tổng quan về Na2S và KOH.
FAQ về Na2S và KOH
- Na2S và KOH có tạo kết tủa khi phản ứng không? (Không)
- Dung dịch Na2S có màu gì? (Không màu)
- KOH có tan trong nước không? (Có)
- Na2S có độc không? (Có thể gây độc nếu nuốt phải hoặc hít phải)
- KOH có nguy hiểm không? (Có thể gây bỏng da và mắt)
- Làm thế nào để bảo quản Na2S và KOH an toàn? (Bảo quản ở nơi khô ráo, thoáng mát, tránh xa tầm tay trẻ em)
- s ra so3 có liên quan gì đến Na2s Koh không? (Không trực tiếp liên quan)
Mô tả các tình huống thường gặp câu hỏi về Na2S và KOH
Sinh viên hóa học thường thắc mắc về phản ứng giữa Na2S và KOH khi học về phản ứng trao đổi ion. Câu hỏi thường gặp là liệu có kết tủa tạo thành hay không.
Gợi ý các câu hỏi khác, bài viết khác có trong web
Bạn đọc có thể tìm hiểu thêm về tính chất của bazơ mạnh và các phản ứng trao đổi ion khác trên trang web Friend LENS.
Kêu gọi hành động
Khi cần hỗ trợ hãy liên hệ Email: [email protected], địa chỉ: Đường Nguyễn Văn Linh, Quận Hải Châu, Đà Nẵng, Việt Nam. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.
