Cu và H2SO4 loãng là hai chất hóa học phổ biến, thường gặp trong các phòng thí nghiệm và ứng dụng công nghiệp. Vậy, khi kết hợp chúng lại với nhau, điều gì sẽ xảy ra? Bài viết này sẽ đi sâu vào phân tích phản ứng (hoặc không phản ứng) giữa Cu và H2SO4 loãng, giúp bạn hiểu rõ bản chất hóa học và các yếu tố ảnh hưởng đến quá trình này.
Cu có tác dụng với H2SO4 loãng không?
Câu trả lời ngắn gọn là: Không. Đồng (Cu) đứng sau Hidro (H) trong dãy điện hóa, nghĩa là Cu có tính khử yếu hơn H+. Do đó, Cu không đủ mạnh để đẩy H+ ra khỏi dung dịch axit loãng như H2SO4. Nói cách khác, phản ứng giữa Cu và H2SO4 loãng sẽ không xảy ra trong điều kiện thường.
Tuy nhiên, nếu H2SO4 ở dạng đặc nóng, phản ứng sẽ diễn ra theo một cơ chế khác, tạo ra sản phẩm khác biệt. Sự khác biệt này nằm ở tính oxi hóa mạnh của H2SO4 đặc nóng, khác với tính axit thông thường thể hiện trong dung dịch loãng.
Tính chất của Đồng (Cu) và Axit Sunfuric Loãng (H2SO4)
Để hiểu rõ hơn về lý do tại sao Cu không phản ứng với H2SO4 loãng, chúng ta cần xem xét tính chất của từng chất. Đồng là kim loại có tính khử tương đối yếu, thường tồn tại ở dạng nguyên chất trong tự nhiên. Trong khi đó, H2SO4 loãng là một axit mạnh, có khả năng phân li hoàn toàn trong nước tạo ra ion H+ và SO42-. Chính ion H+ quyết định tính axit của dung dịch. cus có tác dụng với h2so4 loãng không
Ảnh hưởng của Nồng độ H2SO4
Nồng độ của H2SO4 đóng vai trò quan trọng trong việc xác định liệu phản ứng có xảy ra hay không. Trong trường hợp H2SO4 loãng, nồng độ H+ không đủ cao để oxi hóa Cu. Ngược lại, h2so4 đặc nóng thể hiện tính oxi hóa mạnh, đủ để phản ứng với Cu.
So sánh phản ứng của Cu với H2SO4 loãng và H2SO4 đặc nóng
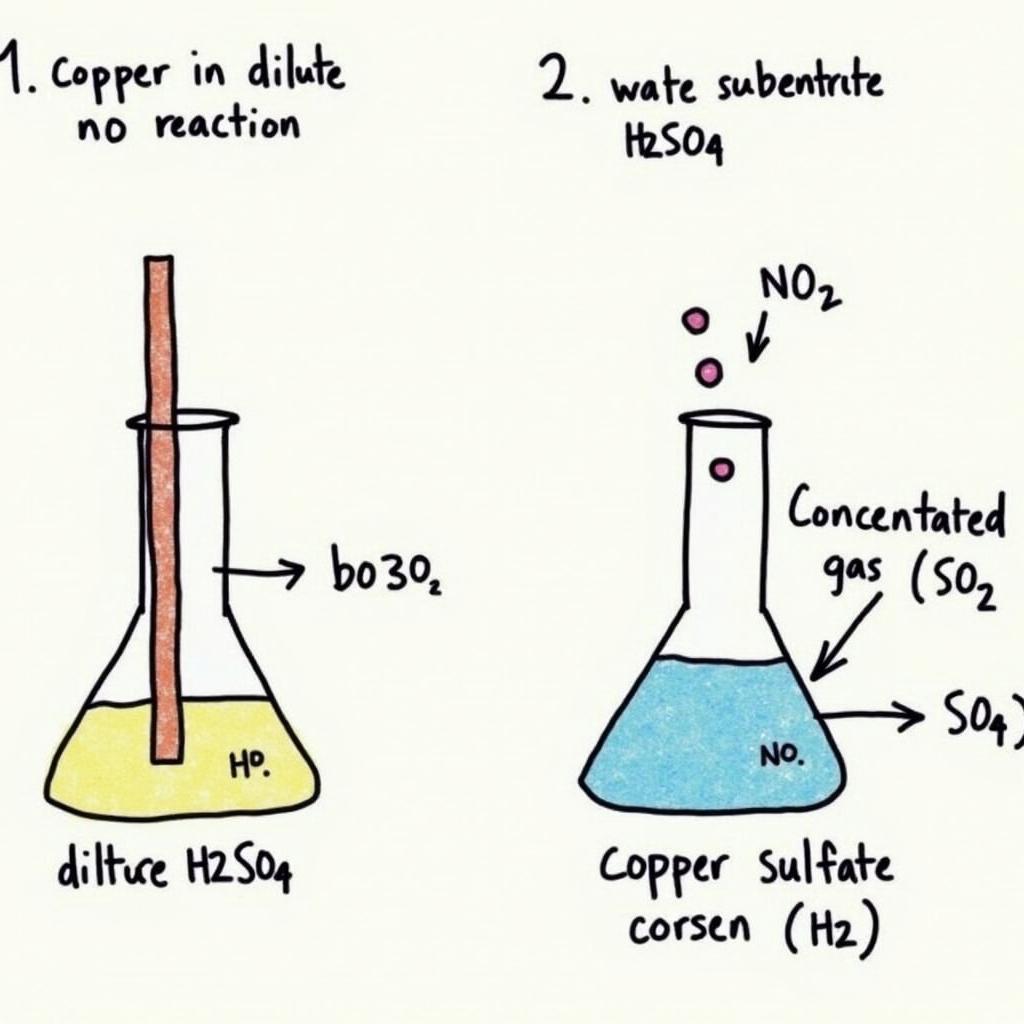 So sánh phản ứng của Cu với H2SO4 loãng và đặc nóng
So sánh phản ứng của Cu với H2SO4 loãng và đặc nóng
Như đã đề cập, Cu không phản ứng với H2SO4 loãng. Tuy nhiên, với H2SO4 đặc nóng, phản ứng sẽ xảy ra tạo thành CuSO4, SO2 và H2O. cu h2so4 đậm đặc
GS. TS. Nguyễn Văn A, chuyên gia hóa học tại Đại học Bách Khoa Hà Nội, cho biết: “Sự khác biệt trong phản ứng của đồng với H2SO4 loãng và đặc nóng nằm ở tính oxi hóa. H2SO4 đặc nóng là chất oxi hóa mạnh, có thể oxi hóa Cu, trong khi H2SO4 loãng thì không.”
Ứng dụng của phản ứng Cu với H2SO4 đặc nóng
Phản ứng giữa Cu và H2SO4 đặc nóng có ứng dụng trong sản xuất CuSO4, một hợp chất quan trọng trong nông nghiệp và công nghiệp.
Điều kiện phản ứng
Để phản ứng giữa Cu và H2SO4 đặc nóng xảy ra, cần đun nóng dung dịch H2SO4 đặc. Nhiệt độ cao giúp tăng cường tính oxi hóa của H2SO4. cu có tác dụng với h2so4 không
PGS. TS. Trần Thị B, Viện Hóa học, cho hay: “Nhiệt độ là yếu tố quan trọng trong phản ứng giữa Cu và H2SO4 đặc. Nếu không đun nóng, phản ứng sẽ không xảy ra hoặc diễn ra rất chậm.”
Kết luận
Tóm lại, Cu không phản ứng với H2SO4 loãng do tính khử yếu của Cu. Chỉ khi H2SO4 ở dạng đặc nóng, phản ứng mới xảy ra tạo thành CuSO4, SO2 và H2O. Hiểu rõ bản chất của phản ứng này giúp chúng ta ứng dụng hiệu quả trong thực tế. chứng minh h2so4 có tính axit
Khi cần hỗ trợ hãy liên hệ Email: [email protected], địa chỉ: Đường Nguyễn Văn Linh, Quận Hải Châu, Đà Nẵng, Việt Nam. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.
