Công Thức Hóa Học Của Phenolphtalein là C₂₀H₁₄O₄. Bài viết này sẽ đi sâu vào tìm hiểu về chất chỉ thị pH quen thuộc này, từ công thức hóa học, tính chất, ứng dụng cho đến những lưu ý khi sử dụng.
Tìm Hiểu Về Phenolphtalein: Từ Công Thức Hóa Học Đến Ứng Dụng
Phenolphtalein (C₂₀H₁₄O₄) là một hợp chất hóa học hữu cơ, được sử dụng rộng rãi như một chất chỉ thị pH trong các thí nghiệm hóa học. Nó có khả năng đổi màu tùy thuộc vào độ pH của dung dịch, giúp xác định tính axit hay bazơ của dung dịch một cách trực quan.
Công Thức Hóa Học Của Phenolphtalein và Cấu Trúc Phân Tử
Công thức hóa học C₂₀H₁₄O₄ cho thấy phenolphtalein được cấu tạo từ 20 nguyên tử cacbon, 14 nguyên tử hydro và 4 nguyên tử oxy. Cấu trúc phân tử của phenolphtalein khá phức tạp, bao gồm ba vòng benzen và hai nhóm hydroxyl. Sự sắp xếp đặc biệt này chính là yếu tố quyết định khả năng đổi màu của phenolphtalein theo pH.
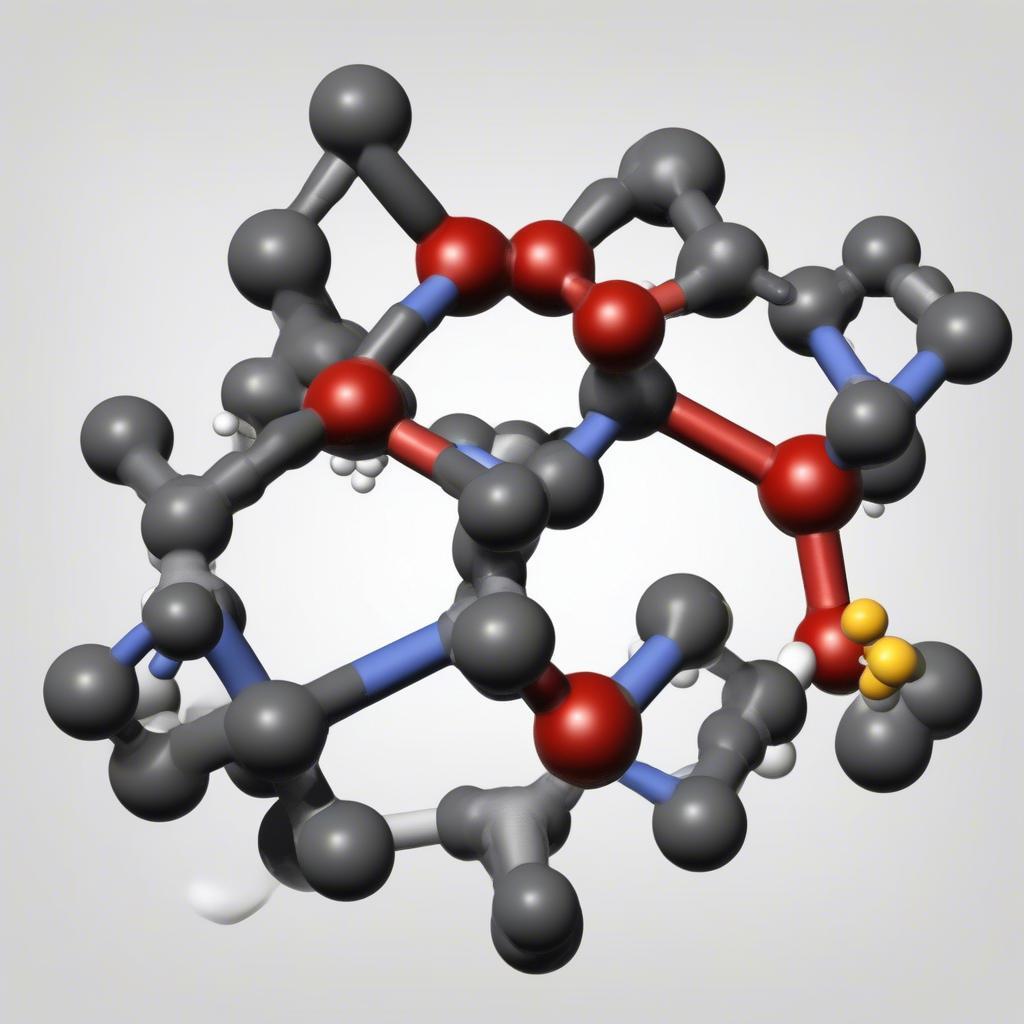 Cấu trúc phân tử của Phenolphtalein
Cấu trúc phân tử của Phenolphtalein
Phenolphtalein Dùng Để Làm Gì?
Ứng dụng phổ biến nhất của phenolphtalein là làm chất chỉ thị trong chuẩn độ axit-bazơ. Trong môi trường axit và trung tính (pH < 8.2), phenolphtalein không màu. Khi pH tăng lên trên 8.2, dung dịch chuyển sang màu hồng, và ở pH rất cao (trên 10), màu hồng chuyển sang màu tím nhạt.
Ngoài ra, phenolphtalein còn được sử dụng trong một số ứng dụng khác như:
- Trong y học: Trước đây, phenolphtalein được sử dụng làm thuốc nhuận tràng. Tuy nhiên, việc sử dụng này đã bị hạn chế do lo ngại về tác dụng phụ tiềm ẩn.
- Trong khoa học hình sự: Phenolphtalein có thể được sử dụng để phát hiện vết máu do khả năng phản ứng với hemoglobin.
- Trong sản xuất đồ chơi: Một số loại mực biến mất sử dụng phenolphtalein để tạo hiệu ứng biến mất và xuất hiện lại.
Cách Sử Dụng Phenolphtalein trong Thí Nghiệm
Khi sử dụng phenolphtalein làm chất chỉ thị, chỉ cần thêm vài giọt dung dịch phenolphtalein vào dung dịch cần kiểm tra. Quan sát sự thay đổi màu sắc để xác định độ pH.
 Sử dụng phenolphtalein trong thí nghiệm
Sử dụng phenolphtalein trong thí nghiệm
Những Lưu Ý Khi Sử Dụng Phenolphtalein
Mặc dù phenolphtalein tương đối an toàn khi sử dụng trong phòng thí nghiệm, vẫn cần lưu ý một số điểm sau:
- Tránh tiếp xúc trực tiếp với da và mắt.
- Không được nuốt.
- Bảo quản ở nơi khô ráo, thoáng mát, tránh ánh sáng trực tiếp.
Công Thức Hóa Học Phenolphtalein và Khả Năng Đổi Màu: Cơ Chế Hoạt Động
Sự đổi màu của phenolphtalein liên quan đến sự thay đổi cấu trúc phân tử của nó khi pH thay đổi. Trong môi trường kiềm, phenolphtalein mất proton, tạo thành anion có màu hồng.
 Cơ chế đổi màu của phenolphtalein
Cơ chế đổi màu của phenolphtalein
Kết luận
Công thức hóa học của phenolphtalein, C₂₀H₁₄O₄, là chìa khóa để hiểu về tính chất và ứng dụng của chất chỉ thị quan trọng này. Từ việc xác định pH trong phòng thí nghiệm đến ứng dụng trong y học và khoa học hình sự, phenolphtalein đóng vai trò không thể thiếu trong nhiều lĩnh vực. Hiểu rõ về công thức hóa học của phenolphtalein giúp chúng ta sử dụng chất này một cách an toàn và hiệu quả.
FAQ
-
Phenolphtalein có độc không?
Phenolphtalein có thể gây kích ứng da và mắt. Việc nuốt phải một lượng lớn có thể gây hại cho sức khỏe.
-
Màu của phenolphtalein trong môi trường axit là gì?
Phenolphtalein không màu trong môi trường axit.
-
Tại sao phenolphtalein đổi màu trong môi trường kiềm?
Do sự thay đổi cấu trúc phân tử và hình thành anion có màu hồng.
-
Phenolphtalein được sử dụng trong những lĩnh vực nào?
Trong chuẩn độ axit-bazơ, y học, khoa học hình sự, và sản xuất đồ chơi.
-
Làm thế nào để sử dụng phenolphtalein an toàn?
Tránh tiếp xúc trực tiếp, không nuốt, và bảo quản đúng cách.
-
Phenolphtalein có phải là chất chỉ thị pH duy nhất không?
Không, có nhiều chất chỉ thị pH khác nhau, mỗi chất có khoảng đổi màu riêng.
-
Công thức hóa học của phenolphtalein là gì?
C₂₀H₁₄O₄
Mô tả các tình huống thường gặp câu hỏi.
Một số tình huống thường gặp câu hỏi về công thức hóa học của phenolphtalein bao gồm học sinh, sinh viên tìm kiếm thông tin cho bài tập, nghiên cứu hoặc các chuyên gia muốn tra cứu lại thông tin.
Gợi ý các câu hỏi khác, bài viết khác có trong web.
Bạn có thể tìm hiểu thêm về các chất chỉ thị pH khác, các phương pháp chuẩn độ axit-bazơ, hoặc các ứng dụng của hóa học trong đời sống.
